钨湿法冶炼过程中,废水产生量大,每生产1t仲钨酸铵产生40~50t废水。废水中主要污染物有COD、氯离子、钠离子、氨氮、砷等。仲钨酸铵生产企业综合废水中氯化钠高达10~20g/L、氨氮80~200mg/L、COD100~500mg/L,废水中盐分高,氨氮属于中低浓度,是典型的高盐氨氮废水。我国在“十二五”期间就已将氨氮纳入了环境污染物约束性控制指标,对冶炼行业废水排放制定了严格的标准,工业废水排放要求氨氮在15mg/L以下。
工业氨氮废水处理的方法主要有物理化学法、生物脱氮法和高级氧化法,常用的物理化学方法有吹脱法、膜技术、吸附法、离子交换法、化学沉淀法、化学氧化法等;生物脱氮法有传统硝化反硝化法、新型的短程硝化反硝化法、同时硝化反硝化法和厌氧氨氧化法等;高级氧化法主要有电化学氧化、臭氧氧化、光催化氧化、催化湿式氧化、折点氯化法等。
尽管去除氨氮的方法很多,但到目前为止仍没有一种去除氨氮的方法能够兼顾流程简单、投资节省、技术成熟、控制方便、无二次污染等优点。物理化学法存在运行成本高、对环境造成二次污染等问题,实际应用受到一定限制;生物脱氮法能较为有效和彻底地去除氨氮,但存在菌种培养较困难,抗负荷能力弱,环境要求高,投资大等问题,也限制其发展;目前,仲钨酸铵结晶工艺产生的高浓度氨氮废水,普遍采用汽提或吹脱工艺降至中低浓度后,与其他中低浓度氨氮废水混合,再采用折点氯化法处理。通过添加含氯氧化剂氧化去除氨氮和COD,然后加入铁盐去除废水中的砷。折点氯化法处理中低浓度的废水具有处理效果好、易操作的优点。但同时也存在氧化剂用量大,运行成本高、环境风险大等问题。
电化学法作为废水处理的一种有效手段,易于控制,成本低,近年来受到了广泛地关注。研究将电化学法引入处理钨冶炼氨氮废水,充分利用冶炼废水中含氯量高的特点,开展电化学法降解钨冶炼废水中低浓度氨氮的研究,以期为后续工业化应用提供技术支持。
1、试验部分
1.1 试验材料
试验废水取自江西某钨冶炼企业生产废水,废水中主要污染物见表1。
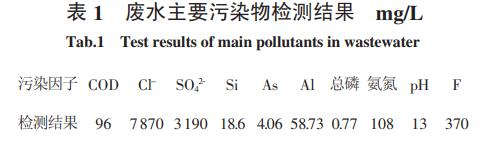
由表1可知,废水中硫酸钠和氯化钠的含量非常高,呈强碱性,无色,且废水有难闻的臭味。主要试剂:氯化钠(分析纯),氯化铵(分析纯),硫酸钠(分析纯),浓硫酸(工业纯)。
1.2 试验装置
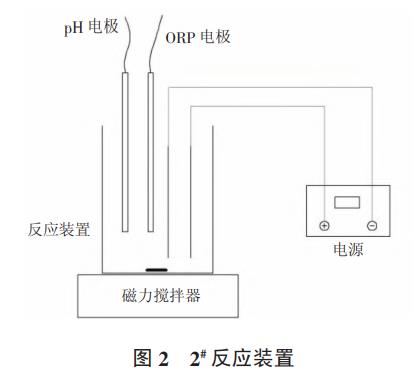
试验采用两种不同的电化学反应装置,分别见图1和图2,根据不同的试验条件选择反应装置。
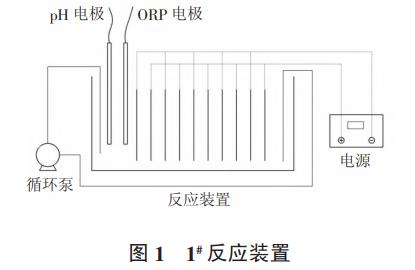
1#反应装置主要用于考察pH、氯离子、硫酸根和电流密度等因素对电化学法降解氨氮的影响。1#反应装置容积为1.2L,采用网孔状析氯电极(Ti/RuO2-IrO2)作为阳极,网孔状钛板为阴极,电极组中包含5块阳极板和5块阴极板,单块电极尺寸均为50mm×50mm。反应装置采用透明有机玻璃材质,尺寸为104mm×104mm×332mm,上部盖板上开设取样孔和电极孔,电极孔用于放置pH电极和ORP电极。采用循环泵搅拌,使溶液混合均匀,直流电源型号WYJ-15V20A,采用稳流模式。
2#反应装置主要用于考察极板间距和不同电极对电化学法降解氨氮的影响。2#反应装置容积为0.3L,包含1块阳极板和1块阴极板,电极尺寸均为50mm×100mm。反应装置长宽高分别为75mm×60mm×135mm,反应装置内刻有等间距的凹槽,凹槽间距为6mm,可根据试验需要更换不同的阳极和调整极板间距,采用磁力搅拌器搅拌,pH、ORP在线检测和电源同1#反应装置。
1.3 基本原理
按照机理的不同,电化学法去除氨氮可分为直接电化学氧化和间接电化学氧化。氨氮直接在阳极表面失去电子被氧化的过程为直接电化学氧化,反应方程式如(1)所示。间接电化学氧化是指氨氮与阳极表面产生的强氧化剂发生氧化还原反应而去除的过程,反应方程式如式(2)~式(4)所示。在一定的条件下,氨氮去除过程中也会发生一些副反应,如阳极析氧反应、阴极析氢反应和氧化剂自身的消耗过程等,反应式方程式如式(5)~式(8)。
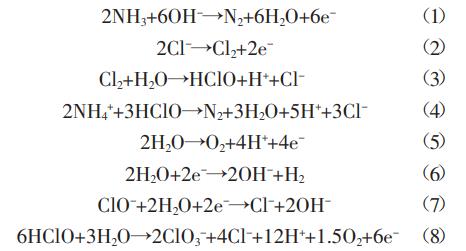
1.4 试验及分析方法
1.4.1 试验方法
单因数条件试验采用模拟废水,模拟废水由去离子水、氯化钠(分析纯)、氯化铵(分析纯)、硫酸钠(分析纯)配置而成,主要成分接近钨冶炼产生的实际废水。单因数条件试验获得的参数通过钨冶炼产生的实际废水进行验证。
以氨氮的去除效率和能耗为评价指标,进行单因数条件试验。使用NaOH或H2SO4调节pH值,在室温条件下进行反应,分别考察pH、电流密度、氯离子浓度、极板间距、电极等影响因数对氨氮去除效率和能耗的影响。反应过程中等时间间隔取样分析氨氮浓度,同时记录电流、电压、pH值、ORP和温度等参数。
1.4.2 分析方法
氨氮采用纳氏试剂分光光度法测定,pH值用pH计(型号PHS-3E)测定,ORP采用ORP计(型号HI2223)测定。
1.4.3 能耗计算
能耗计算公式如式(9)所示:
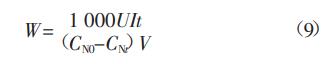
式中:W为电化学过程单位氨氮降解的电耗,kW·h/kg;I为电流,A;U为电压,V;t为反应时间,h;CN0为反应前氨氮浓度,mg/L;CNt为反应时间为t时的氨氮浓度,mg/L;V为废水体积,L。
2、试验结果与分析
2.1 反应初始pH值的影响
采用1#反应装置,配置模拟废水1.2L,氨氮浓度200mg/L,极板间距18mm,氯离子浓度8g/L,电流密度200A/m2,分别调节不同的pH值,每隔5min取样一次,检测氨氮浓度,分析不同初始pH值对氨氮去除效率和能耗的影响,结果如图3、图4、图5所示。
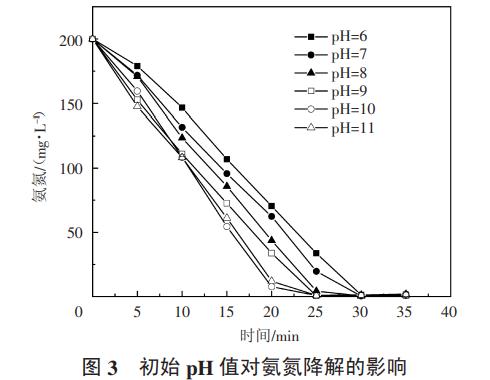
由图3可知,随着初始pH值的升高,氨氮降解速度加快。初始pH=10时氨氮去除效率达到最大;当初始pH=11时,氨氮去除效率略有降低。这是因为氨氮在酸性条件下,主要以NH4+形式存在,而NH4+比NH3更难通过电化学反应降解,另外,在酸性条件下,反应产生的有效氯容易转化成氯气溢出,导致溶液中有效氯降低。氯气的溶解度随着初始pH值的增加而增加,但是强碱性条件下,氯气在水中会发生歧化反应,部分氯气转化成高氯酸,而高氯酸与氨氮几乎不发生反应,导致氨氮的去除效率也降低。
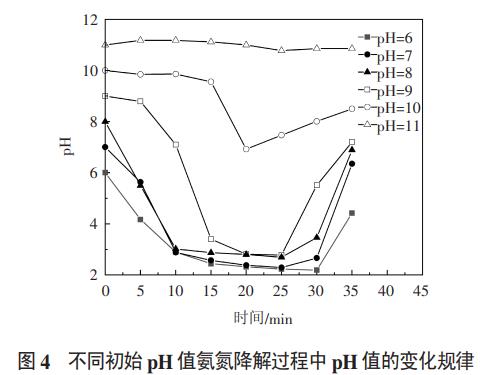
图4显示了不同初始pH值反应过程中pH值的变化规律。不同初始pH值的废水在反应过程中pH值均呈现先降低再升高的规律,废水初始pH值越低,下降到最低点时的pH值也越低。这是因为氨氮在电化学反应降解过程中会产生H+,氨氮的降解过程也就是pH值下降的过程,理论上pH值降到最低点时,氨氮降解完全。氨氮降解完全后,继续反应产生的氢气和过饱和氯气溢出,废水中的OH不断累积,导致pH值慢慢升高。
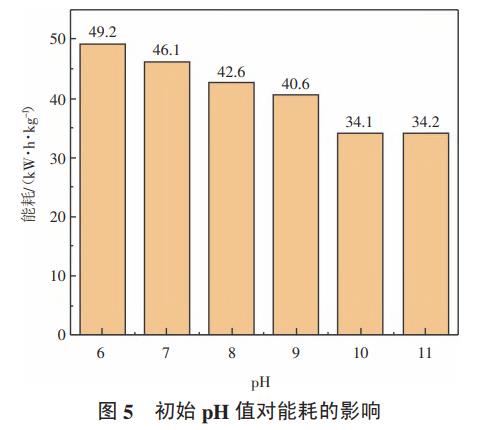
由图5可知,随着初始pH值的升高,去除单位氨氮的能耗先快速下降,后略有升高,能耗从初始pH=6时的49.2kW·h/kg高点逐渐降到pH=10时的34.1kW·h/kg最低点,这是因为pH越低,反应产生的氯气越容易溢出,导致废水中有效氯减少。当初始pH大于10后,能耗略有上升。据相关文献报道,碱性条件下氨氮降解的产物中除了氮气外,还含有一定量的硝态氮和亚硝态氮,且碱性越强,硝态氮和亚硝态氮的比例也越高,因此,强碱性条件下反应可能会导致总氮偏高。
综合考虑氨氮的降解效率和能耗,pH过低会导致反应产生的氯气溢出,pH过高会发生歧化反应,且会导致总氮偏高,因此,降解氨氮最佳pH值应控制在9~10之间。
2.2 氯离子的影响
采用1#反应装置,配置模拟废水1.2L,氨氮浓度200mg/L,电流密度200A/m2,极板间距18mm,初始pH=9,分别调节不同的氯离子浓度,每隔5min取样一次,检测氨氮浓度,分析氯离子浓度对氨氮去除效率和能耗的影响。结果如图6、图7所示。
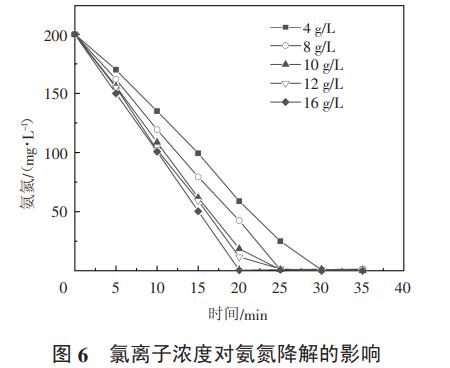
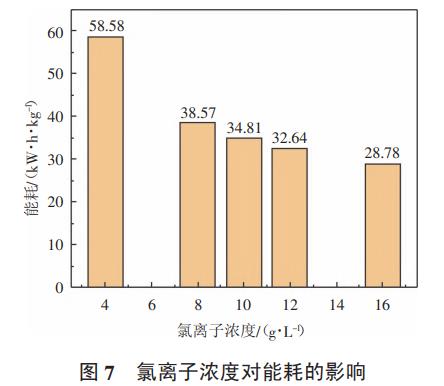
从图6可以看出,在其他条件相同的情况下,随着氯离子浓度的增加,氨氮的降解速率也加快,结合图7可知,随着氯离子的增加,同样能耗也下降,但是能耗下降幅度逐渐收窄,说明氯离子浓度继续增加对能耗下降幅度有限。
在电化学反应过程中氯离子与氨氮反应以间接氧化为主,氯离子在溶液中具有两个作用:一是氯离子作为支持电解质,提高溶液的导电能力,降低电能消耗;二是作为电极反应物,有利于降低氧气析出,提高氯气析出的电流效率,从而增加活性氯(主要是氯气、次氯酸和次氯酸根)的产生量,促进氨氮的氧化。
随着氯离子浓度的增加,废水电导率也增加,槽电压下降导致降解单位质量的氨氮所消耗的能耗降低,能耗最低可降至28.78kW·h/kg;随着氯离子浓度的增加,活性氯生成速度加快,氯离子浓度从4g/L增加至16g/L,氨氮完全降解时间由30min降至约20min。故在氯离子浓度升高到一定程度后氨氮降解速率增加不明显。
2.3 电流密度的影响
采用1#反应装置,配置模拟废水1.2L,氨氮浓度200mg/L,氯离子8g/L,极板间距18mm,初始pH=9,分别调节不同的电流密度,每隔5min取样一次,检测氨氮浓度,分析电流密度对氨氮去除效率和能耗的影响。结果如图8、图9所示。
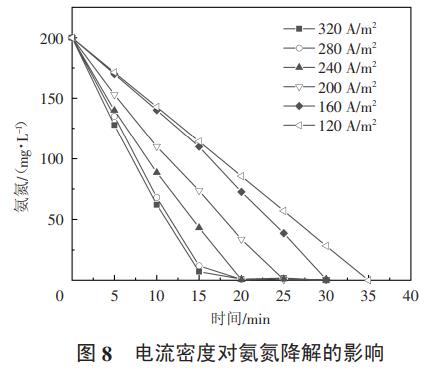
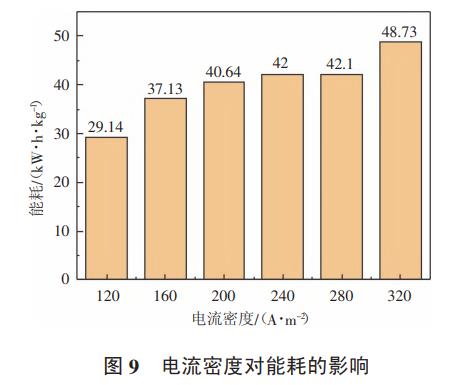
从图8和图9可以看出,随着电流密度的增加,氨氮的降解速率逐渐加快,氨氮完全降解的时间从35min降至约15min,而能耗随着电流密度的增加而降低。当电流密度为120A/m2时,氨氮降解的能耗为29.14kW·h/kg。
活性氯的产生与电流密度密切相关,电流密度越大,单位时间内产生的有效氯越多,反之越少,所以电流密度对氨氮的降解速度影响极大。在电化学反应中,电压是驱动力,电流则表示反应的快慢程度,增加电流密度,槽电压也相应增加,当电压增加到析氧电位时,阳极可同时发生析氯和析氧反应,提高电流密度,阳极上加快析氯的同时,副反应析氧速率同时也加快。当电流密度120A/m2时,电极反应速率最慢,电压也最低,同时,析氧副反应少,因此能耗也更低。当提高电流密度到320A/m2后,槽电压明显升高,同时也加快了副反应的发生,导致氨氮降解能耗增加到48.73kW·h/kg。小电流密度虽然能节省能耗,但反应速度慢,需要增大设备投资成本;电流密度过大,反应速度快,设备投资成本低,但是能耗高。因此,在实际应用过程中,要综合考虑氨氮降解速度,能耗和处理效果之间的关系,确定最佳的电流密度。后期试验均采用200A/m2的电流密度。
2.4 极板间距的影响
采用2#反应装置,配置模拟废水0.3L,氨氮浓度200mg/L,氯离子8g/L,电流密度200A/m2,初始pH=9,分别调节不同的极板间距,每隔5min取样一次,检测氨氮浓度,分析极板间距对氨氮去除效率和能耗的影响。结果如图10、图11所示。
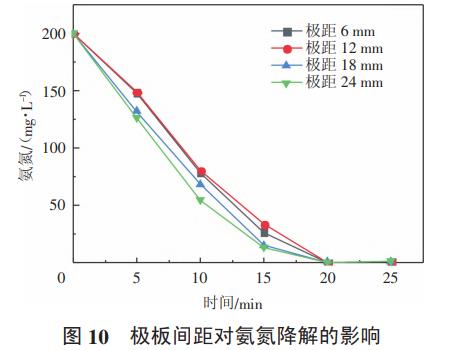
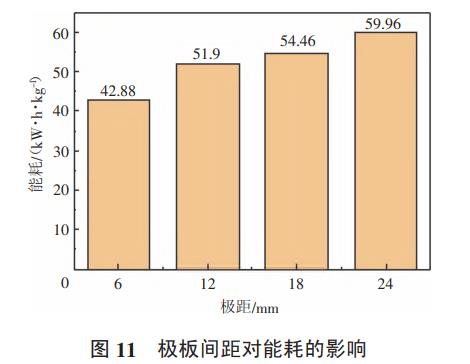
极板间距是影响氨氮降解的另一个重要因数,从图10和图11可以看出极板间距从6mm增加到24mm,氨氮的降解速率也逐渐增加,但是增加的幅度较小,氨氮降解能耗随着极板间距的增加而增加,说明极板间距对氨氮的降解速率影响不大,而对能耗的影响较大,适当缩小极板间距有利于降低能耗。试验结果与文献的类似,当极板间距减小到一定程度后,阳极产生的有效氯很容易到达阴极表面发生还原反应,从而降低有效氯的浓度,导致氨氮降解速度略有降低;继续加大极板间距后,发生副反应的概率逐渐降低,但是氯离子的迁移路径更长,阴阳极之间电阻增大,电压升高,部分电能转化成热能,从而导致能耗增加。
2.5 电极的影响
采用2#反应装置,配置模拟废水0.3L,氨氮浓度200mg/L,氯离子8g/L,电流密度200A/m2,初始pH=9,极距12mm,分别采用不同的阳极,每隔5min取样一次,检测氨氮浓度,分析不同电极对氨氮去除效率和能耗的影响,结果如图12、图13所示。
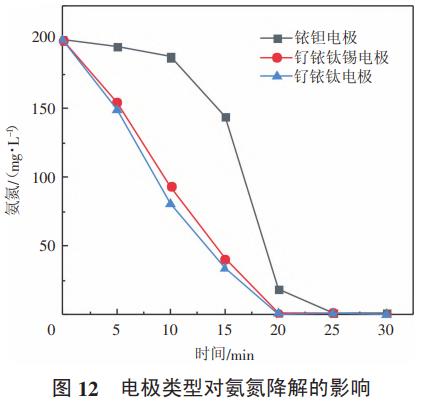
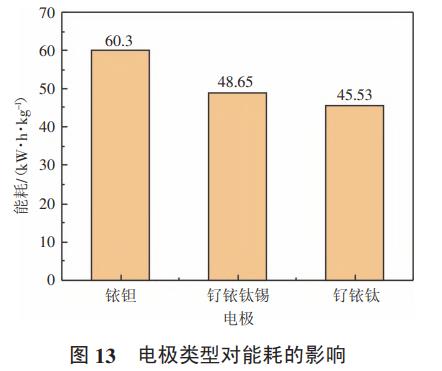
电极在电化学反应系统中起到决定性的作用,需要根据不同的目的选择相应的电极。依据电化学降解氨氮的需要,宜选择析氯电位低且析氧电位高的电极,含有铱涂层的电极具备该特性,因此试验中选用3种含有铱涂层的电极进行对比试验。从图12中可以看出,铱钽电极作为阳极时,氨氮前期降解速度非常慢,后期降解速度迅速加快;而钌铱钛锡电极和钌铱钛电极作为阳极时,氨氮降解速率相对稳定,且降解速率非常接近。图13显示三种电极中钌铱钛电极做阳极时能耗最低,去除1kg氨氮的能耗为45.53kW·h;钌铱钛锡电极能耗为48.65kW·h/kg,与钌铱钛电极接近;铱钽电极能耗最高,达到60.3kW·h/kg。
1#反应装置和2#反应装置中的电极采购自不同的厂家,1#反应装置采用多块阳极和多块阴极组成的电极组,2#反应装置为单块阳极和单块阴极组成。从前面的试验可以发现1#反应装置的能耗普遍低于2#反应装置,说明电极涂层中各元素的配比和电极的组合形式都会影响氨氮降解过程中的能耗。
2.6 硫酸根的影响
采用1#反应装置,配置模拟废水1.2L,氨氮浓度200mg/L,氯离子8g/L,电流密度200A/m2,初始pH=9,极距18mm,钌铱钛阳极,每隔5min取样一次,检测氨氮浓度,分析不同浓度的硫酸根对氨氮去除效率和能耗的影响。结果如图14、图15所示。
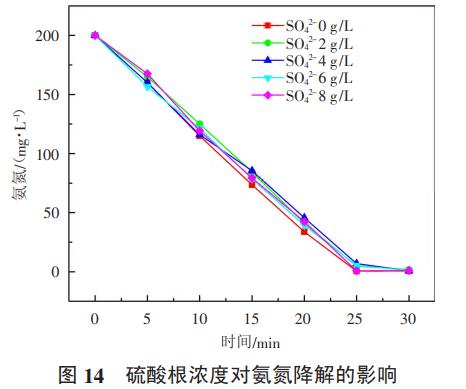
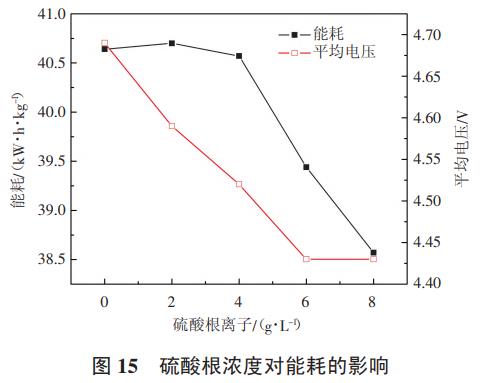
由图14可知,其他条件不变,废水中硫酸根浓度从0g/L逐渐增加到8g/L,氨氮的降解速率略有降低,但降低幅度不明显。从图15中可以看出废水中的硫酸根浓度在0~6g/L之间时,随着硫酸根浓度的增加平均电压逐渐降低,当废水中硫酸根浓度大于6g/L后,平均电压维持稳定,当硫酸根浓度在0~4g/L之间时,随着硫酸根浓度增加,单位氨氮降解能耗几乎不变,而当硫酸根浓度在大于4g/L后,单位氨氮降解的能耗逐渐降低。硫酸根本身不参与电化学反应,但硫酸根阴离子会向阳极表面富集,硫酸根浓度越大阳极表面富集的硫酸根越多,阻碍了氯离子向阳极的迁移,阳极表面固液界面电阻增加,表现出电压增加,并降低氨氮的降解效率,当硫酸根浓度在6g/L左右时,阳极表面的富集硫酸根达到饱和,继续增大硫酸根浓度,阳极表面电阻不变,但因硫酸根是强电解质,可增加废水的电导率,降低阴阳极之间的溶液电阻,对氨氮降解过程产生促进作用。因此,硫酸根对氨氮降解能耗具有正、负两方面的作用,硫酸根浓度小于4g/L时,正负作用相互抵消,而大于4g/L时,硫酸根的存在有利于降低氨氮降解能耗。
2.7 实际废水氨氮降解试验
采用1#反应装置,取钨冶炼废水1.2L,氨氮浓度为108mg/L,电流密度为200A/m2,初始pH=9,极距为18mm,钌铱钛电极为阳极,每隔3min取样一次,检测氨氮浓度,分析实际废水中氨氮降解和能耗的规律。结果如图16所示。
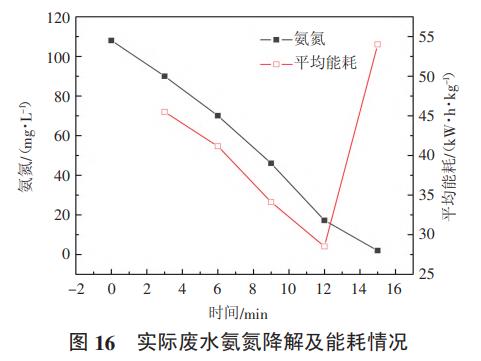
从图16中可以看出,实际钨冶炼废水中氨氮的降解曲线与模拟废水的降解曲线类似,均为零级反应,随着反应的持续进行,废水中的氨氮浓度呈现匀速下降趋势,反应15min后,氨氮浓度可降低到小于1mg/L。能耗随着氨氮的降解先降低后升高,这是因为反应前期,废水中有效氯浓度低,氨氮降解速率慢,随着反应的继续进行,废水中有效氯浓度逐渐升高,体现在能耗上就是逐渐降低的趋势。反应15min时能耗突然升高,反应15min时的能耗为12~15min之间的平均能耗。出现该现象的原因是反应12~15min时氨氮已降解完全,由于超过了反应终点取样,相同时间里氨氮降解量少,导致平均能耗升高。经计算,实际废水电化学反应全过程中氨氮降解平均能耗为38.7kW·h/kg。
3、结论
通过电化学降解模拟废水中氨氮的研究可知,弱碱性条件下有利于氨氮的降解,初始pH=10左右单位氨氮降解的能耗最低;废水中氯离子浓度越高氨氮的降解速率越快,且氨氮降解能耗也更低;电流密度对反应速率起决定性作用,电流密度越大,氨氮降解速率越快,单位氨氮降解的能耗也越高;极板间距在6~24mm之间时,缩短极板间距有利于加快反应速度和降低能耗;比较了铱钽电极、钌铱钛锡电极和钌铱钛电极三种电极性能,其中钌铱钛电极在降解速率和能耗方面都好于其他两种电极;废水中硫酸根的存在对氨氮的降解速率有一定影响,硫酸根能降低废水中的电阻,从而降低能耗,6g/L的硫酸根能降低能耗5.8%。
通过对钨冶炼产生的实际废水进行验证试验可知,实际废水氨氮降解规律与模拟废水类似,采用钌铱钛阳极、电流密度200A/m2、初始pH=9,极板间距18mm,初始氨氮浓度108mg/L条件下,反应15min,废水中氨氮浓度可降低到1mg/L以下,氨氮降解能耗为38.7kW·h/kg。(来源:赣州有色冶金研究所有限公司)



